Moderna poinformowała, że jej szczepionka przeciw COVID-19 wywołała silną odpowiedź immunologiczną i była ogólnie dobrze tolerowana u dzieci w wieku od 6 do 11 lat. Firma planuje wkrótce przekazać dane organom regulacyjnym. We wtorek Amerykańska Agencja Żywności i Leków ma zadecydować o dopuszczenu dla dzieci w wieku 5-11 lat szczepionki innej firmy, Pfizera.Moderna przekazała, że efekty podania jej dwudawkowej szczepionki dla dzieci w wieku 6-11 lat były porównywalne z tym, co wcześniej zaobserwowano w badaniach klinicznych z udziałem młodzieży i dorosłych.
OGLĄDAJ TVN24 W INTERNECIE W TVN24 GO
Koncern poinformował także, że większość niepożądanych objawów w badaniu, w którym wzięło udział 4753 uczestników, miała charakter łagodny lub umiarkowany. Najczęstszymi obajwami tego typu były zmęczenie, ból głowy, gorączka i ból w miejscu wstrzyknięcia.
Szczepionki zastosowane w badaniu miały dawki 50 mikrogramów, co stanowi połowę mocy stosowanej w podstawowej serii szczepionek dla dorosłych.
Szczepionka Pfizera dla dzieci w wieku 5-11 lat
Wcześniej Amerykańska Agencja Żywności i Leków (FDA) wydała analizę badań nad szczepionkami przeciw COVID-19 firmy Pfizer/BioNTech dla dzieci w wieku 5-11 lat. Jak poinformowano, preparaty wykazują dużą skuteczność w zapobieganiu objawowym infekcjom u dzieci i nie spowodowały żadnych nieoczekiwanych problemów. Eksperci FDA we wtorek mają podjąć decyzję o zatwierdzeniu szczepionki.
Koronawirus na świecie
Źródło: TVN24
Nagły wzrost liczby zakażonych brytyjskim wariantem koronawirusa w regionie paryskim
Teraz oglądasz
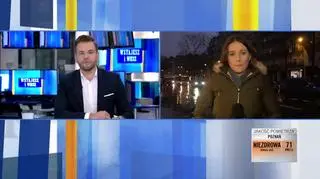
Nowy lockdown w Anglii. Relacja korespondenta "Faktów TVN"
Ambasador RP w Londynie o sytuacji w Dover

Teraz oglądasz
Korespondent TVN24 o szczepieniach w Unii Europejskiej i apelu szefowej KE Ursuli von der Leyen

Teraz oglądasz
"To, że nastąpiło to tak szybko, jest ogromnym sukcesem"

Teraz oglądasz
Stadiony zmienione w szpitale na świecie

Teraz oglądasz
Polka mieszkająca w Pradze: widać między ludźmi, że się boją

Teraz oglądasz
Roksana Guillen Ortega, Polka mieszkająca w Hiszpanii, o powrocie do lockdownu między innymi w Madrycie
Teraz oglądasz
"Krytycy wykazują olbrzymią ilość sprzeczności"
Ogromny wzrost zakażeń w Wielkiej Brytanii

Teraz oglądasz
Kary za brak maseczki ochronnej w poszczególnych krajach

Teraz oglądasz
Kwarantanna dla wszystkich przybywających z Hiszpanii na Wyspy Brytyjskie

Teraz oglądasz
Godzina policyjna w Antwerpii z powodu pandemii
Johnson: mam nadzieję, że będziemy mogli umożliwić znaczący powrót do normalności najwcześniej od listopada

Teraz oglądasz
Pierwsza dama Ukrainy, u której zdiagnozowano COVID-19, trafiła do szpitala

Teraz oglądasz
Węgierski parlament przyjmuje kontrowersyjne ustawy
Hodowla norek

Teraz oglądasz
Dwa uniwersytety w Wielkiej Brytanii będą uczyć tylko zdalnie do końca przyszłego roku akademickiego

Teraz oglądasz
Komisja Europejska przedstawia rekomendacje w sprawie otwarcia granic wewnętrznych UE

Teraz oglądasz
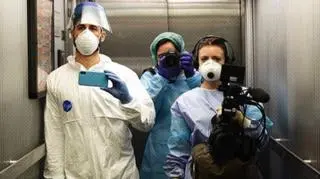
Włoscy dziennikarze na froncie walki z koronawirusem
Teraz oglądasz
Dr Krowicka o luzowaniu ograniczeń w Czechach
Teraz oglądasz
Wojciechowski: pierwszą syrenę alarmową Komisja Europejska uruchomiła 9 stycznia
Teraz oglądasz
Raport z Rosji korespondenta "Faktów" Andrzeja Zauchy

Teraz oglądasz
Raport z Niemiec korespondenta Radia ZET, Wojciecha Hernesa

Teraz oglądasz
Polscy lekarze pomagali we Włoszech

Teraz oglądasz
Nieznane źródło zakażenia koronawirusem na lotniskowcu Charles de Gaulle
Szefowa KE o strategii wyjścia z ograniczeń wprowadzonych w związku pandemią
Teraz oglądasz
"Od kilku dni obserwujemy spadek przyjęć do szpitala"

Teraz oglądasz
Polska pielęgniarka z Malmo: Największa epidemia dzieje się w Sztokholmie. Tam prawdopodobnie brakuje większości rzeczy

Teraz oglądasz
Polska pielęgniarka z Szwecji opowiada o pracy w szpitalu

Teraz oglądasz
Polska pielęgniarka z Malmo: statystyki wpływają na moją psychikę, stresuję się chodzeniem do pracy

Teraz oglądasz
We Włoszech został opracowany nowy test serologiczny

Teraz oglądasz
Jacek Stawiski o sytuacji w niemieckich domach pomocy społecznej

Teraz oglądasz
Polski lekarz we Włoszech: przyrost chorych i przypadków śmiertelnych maleje

Teraz oglądasz
Autorka/Autor: mjz\mtom
Źródło: Reuters